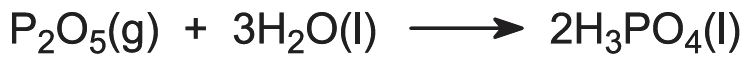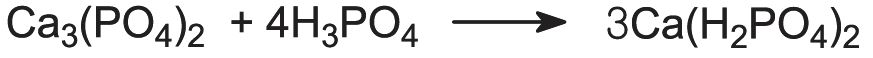Zastosowanie kwasu fosforowego
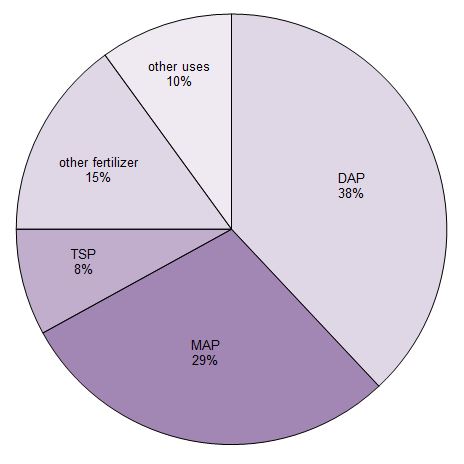
Około 90% produkowanego kwasu fosforowego jest wykorzystywane do produkcji nawozów. Jest on głównie przekształcany w trzy sole fosforanowe, które są stosowane jako nawozy. Są to superfosfat potrójny (TSP), wodorofosforan diamonu (DAP) i dwuwodorofosforan monoamonowy (MAP).
Rysunek 1 Zastosowania kwasu fosforowego.
Dane z Potash Corporation, 2014
Fosforany są również wykorzystywane na wiele innych sposobów, w tym w napojach bezalkoholowych i jako dodatek do paszy podawanej bydłu, trzodzie chlewnej i drobiowi.
Ale chociaż w wielu krajach wycofano się z ich stosowania jako budulców w detergentach, to w niektórych krajach nadal jest to ważne zastosowanie tego kwasu.
Roczna produkcja kwasu fosforowego
| Świat | 43 mln ton1,2,3 |
| Chiny | 17 mln ton4 |
| Południowo-wschodnia i północno-wschodnia Azja | 10 mln ton4 |
| USA | 8.4 mln ton5 |
1 Potash Corporation, 2014
2 JDCPhosphate, 2014
3 Szacunki na 2016
4 Ekstrapolowane na podstawie danych, IHS,Markit, 2015
5 2015 Business of Chemistry, American Chemistry Council, 2016
Produkcja kwasu fosforowego
Kwas fosforowy powstaje w dwóch procesach:
a) proces „mokry”
b) proces termiczny
Metoda termiczna daje zwykle bardziej skoncentrowany i czystszy produkt, ale jest energochłonna (ze względu na wytwarzanie samego fosforu. Kwas produkowany metodą „mokrą” jest mniej czysty, ale jest używany do produkcji nawozów.
(a) Proces mokry
Kwas fosforowy jest produkowany z fluorapatytu, znanego jako skała fosforytowa, 3Ca3(PO4)2.CaF2, przez dodanie stężonego (93%) kwasu siarkowego w serii dobrze wymieszanych reaktorów. W wyniku tego powstaje kwas fosforowy i siarczan wapnia (gips) oraz inne nierozpuszczalne zanieczyszczenia. Dodawana jest woda, a gips jest usuwany przez filtrację wraz z innymi nierozpuszczalnymi materiałami (np. krzemionką). Fluorki, jako H2SiF6, są usuwane na dalszym etapie przez odparowanie.
Pomimo, że reakcja przebiega etapami z udziałem dwuwodorofosforanu wapnia, ogólną reakcję można przedstawić jako:
Jednakże występują reakcje uboczne; na przykład z fluorkiem wapnia i węglanem wapnia obecnym w skale:


Kwas fluorokrzemowy jest ważnym produktem ubocznym tego procesu oraz produkcji fluorowodoru. Może być neutralizowany wodorotlenkiem sodu, tworząc heksafluorokrzemian sodu. Kwas ten jest również używany do produkcji fluorku glinu, stosowanego z kolei w produkcji aluminium.
Struktura krystaliczna powstałego siarczanu wapnia zależy od warunków reakcji. W temperaturze 340-350 K głównym produktem jest dwuwodzian, CaSO4.2H2O. W temperaturze 360-380 K powstaje półwodzian, CaSO4.1/2H2O.
Siarczan wapnia jest odfiltrowywany, a następnie kwas jest zatężany do około 56% P2O5 za pomocą destylacji próżniowej.
Produkt z kwasu otrzymany w procesie mokrym jest nieczysty, ale może być użyty, bez dalszego oczyszczania, do produkcji nawozów (patrz poniżej). Ewentualnie można go dalej odparować do ok. 70% P2O5, roztworu zwanego kwasem superfosforowym, który jest stosowany bezpośrednio jako płynny fertygator.
Do produkcji fosforanów przemysłowych kwas oczyszcza się przez ekstrakcję rozpuszczalnikową, stosując np. keton metylowo-izobutylowy (MIBK), w którym kwas jest słabo rozpuszczalny, i zatęża do 60% zawartości P2O5. Kwas ten może być dalej oczyszczany przy użyciu rozpuszczalników w celu usunięcia metali ciężkich i odfluorowany (przez odparowanie), aby otrzymać produkt o jakości spożywczej.
(b) Proces termiczny
Surowcami w tym procesie są fosfor i powietrze:
Początkowo fosfor jest rozpylany do pieca i spalany w powietrzu w temperaturze około 1800-3000 K.
Większość procesów wykorzystuje nieosuszone powietrze, a wiele z nich obejmuje dodawanie pary do palnika fosforowego w celu wytworzenia i utrzymania warstwy skondensowanych kwasów polifosforowych, które chronią wieżę palnika ze stali nierdzewnej (chłodzoną zewnętrznie wodą). Produkty z wieży palnika przechodzą bezpośrednio do wieży hydratacyjnej, gdzie gazowy tlenek fosforu jest absorbowany w przetworzonym kwasie fosforowym:
Alternatywnie, fosfor może być spalany w osuszonym powietrzu. Pięciotlenek fosforu jest skraplany jako biały proszek i oddzielnie uwodniony do kwasu fosforowego.
Ta metoda pozwala na odzyskanie ciepła i ponowne wykorzystanie.
Spalanie i bezpośrednie uwodnienie, jak opisano wcześniej, stwarza wysoce korozyjne warunki. Urządzenia są zbudowane ze stali nierdzewnej lub są wyłożone cegłą węglową. Aby zmniejszyć korozję, ściany palnika i wieże hydratora są chłodzone, ale produkty reaktora pojawiają się w temperaturze zbyt niskiej do użytecznego odzysku ciepła.
Kwas produktowy ma stężenie około 85%.
Kwas tetrafosforowy, jeden z rodziny kwasów polifosforowych, które mogą być selektywnie produkowane, jest wytwarzany albo przez gotowanie wody w wysokiej temperaturze w naczyniu węglowym, lub przez dodanie stałego pięciotlenku fosforu do prawie wrzącego kwasu fosforowego. Pierwsza metoda zwykle daje czystszy produkt, ze względu na wysoką zawartość arsenu w pięciotlenku fosforu.
Fosforany
Sole kwasu fosforowego, fosforany, są związkami, które są szeroko stosowane w rolnictwie, przemyśle i w domu.
(a) Fosforany amonowe
Dwuwodorofosforan monoamonowy i wodorofosforan dwuamonowy są szeroko stosowane jako nawozy i są wytwarzane przez mieszanie właściwych proporcji kwasu fosforowego z bezwodnym amoniakiem w obracającym się bębnie.
Wybór fosforanu amonu do użycia zależy od proporcji azotu i fosforu potrzebnych do uprawy.
(b) Fosforany wapnia
Fosforany wapnia są szeroko stosowane jako nawozy. Dwuwodorofosforan wapnia, Ca(H2PO4)2, jest wytwarzany w reakcji fosforanu z kwasem siarkowym:
Znany jest jako superfosfat. Zawiera on około 20% P2O5.
Jeśli skała fosforytowa jest poddawana działaniu kwasu fosforowego, a nie kwasu siarkowego, powstaje bardziej skoncentrowana forma dwuwodorofosforanu wapnia o ogólnie wyższym poziomie P2O5 (50%):
Jest on znany jako superfosfat potrójny. Wyższy poziom fosforanu uzyskuje się dzięki temu, że produkt nie jest już rozcieńczany siarczanem wapnia.
(c) Fosforany sodu
Fosforany sodu powstają w wyniku reakcji kwasu fosforowego i stężonego roztworu wodorotlenku sodu w odpowiednich (stechiometrycznych) proporcjach. Produkt ulega krystalizacji.
- Dwuwodorofosforan monosodowy (MSP, NaH2PO4) jest stosowany w preparatach do czyszczenia metali i przygotowania powierzchni, jako źródło fosforanów w produkcji farmaceutycznej, a także jako środek regulujący pH w pastach do zębów, w emalii szklistej (wyroby sanitarne) oraz w produkcji fosforanów skrobiowych. Jednym z największych zastosowań jest uzdatnianie wody pitnej. Albo kwas fosforowy lub MSP może być stosowany do wytwarzania cienkiej nierozpuszczalnej powłoki fosforanu ołowiu na rurach ołowianych, aby zapobiec rozpuszczeniu ołowiu przez kwasy w wodzie.
- Wodorofosforan disodowy (Na2HPO4) jest stosowany jako środek zmiękczający w serze topionym, w emaliach i szkliwach ceramicznych, w garbowaniu skóry, w produkcji barwników i jako inhibitor korozji w uzdatnianiu wody.
- Fosforan trisodowy (Na3PO4) jest stosowany w ciężkich środków czyszczących, na przykład w odtłuszczania stali. Jest zasadą i sekwestrantem dla jonów wapnia, utrzymując je w roztworze i zapobiegając tworzeniu się szumowin.
- Pirofosforan disodowy (Na2H2P2O7) jest używany jako zaczyn w chlebie/ciastach (pomaga w uwalnianiu dwutlenku węgla z sody oczyszczonej), jako środek hamujący powstawanie tlenku żelaza (efekt ciemnienia lub brązowienia) w produkcji różnych produktów spożywczych i jako dyspergator w płuczce wiertniczej do odwiertów naftowych.
.