WPROWADZENIE
W różnych badaniach epidemiologicznych wykazano, że przewlekła choroba nerek (CKD) stanowi istotny problem zdrowia publicznego.1-6 Jej obecność wiąże się z dużym ryzykiem wystąpienia schyłkowej przewlekłej choroby nerek, chorób układu sercowo-naczyniowego i zgonu.7 Dane z badania EPIRCE wskazują, że częstość występowania CKD, za którą uważa się sytuację, w której współczynnik filtracji kłębuszkowej (GFR) wynosi poniżej 60 ml/min/1,73 m2 (stadia 3-5 bez dializoterapii), wynosi 6,5% populacji hiszpańskiej w wieku powyżej 18 lat.8-10 Najlepszym wskaźnikiem do pomiaru czynności nerek jest GFR. Biorąc pod uwagę, że pomiar klirensu inuliny bezpośrednio lub metodami izotopowymi jest skomplikowany, kosztowny i nie może być stosowany w codziennej praktyce, popularne stały się szacunki GFR oparte na równaniach wykorzystujących kreatyninę w surowicy i inne zmienne, takie jak wiek, płeć, grupa etniczna i powierzchnia ciała.11-13 Równania te poprawiają słabą korelację, jaka występuje między kreatyniną a GFR. Obecnie większość towarzystw medycznych,14-22 w tym Hiszpańskie Towarzystwo Nefrologiczne (SEN) oraz Hiszpańskie Towarzystwo Biochemii Klinicznej i Patologii Molekularnej (SEQC), zaleca stosowanie równania z badania MDRD (Modification of Diet in Renal Disease) do szacowania GFR; zalecenie to pojawiło się w dokumencie Consensus Document dotyczącym szacowania filtracji kłębuszkowej, który nasza grupa pomogła przygotować.14 Stwierdza się w nim, że MDRD należy stosować pod warunkiem oznaczania kreatyniny w surowicy metodą klasyczną (MDRD-4) lub preferowaną metodą MDRDIDMS, w zależności od tego, czy metoda analityczna stosowana do oznaczania kreatyniny jest identyfikowalna z metodą referencyjną przy użyciu spektrometrii mas z rozcieńczeniem izotopowym (IDMS).15 Jednak takie czynniki, jak populacja, z której pochodzi wzór (pacjenci z określonym stopniem zaawansowania CKD), oraz trudności związane z brakiem standaryzacji pomiaru kreatyniny w surowicy (których rozwiązanie jest na zaawansowanym etapie) stanowią problem w jego stosowalności. Podawanie dokładnej wartości liczbowej dla wyników GFR powyżej 60 lub 90 ml/min/1,73m2 nie jest zalecane, w zależności od przewodnika praktyki klinicznej, z którym się konsultujemy.14-23 Z tego samego powodu opowiadamy się za potrzebą poszukiwania nowych markerów funkcji nerek lub nowych równań do szacowania GFR, które dawałyby lepsze wyniki niż MDRD. CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) jest grupą badawczą działającą w ramach amerykańskiego National Institute of Diabetes and Digestive and Kidney Disease (NIDDK). Powstała ona w celu opracowania i walidacji równań szacowania GFR na podstawie danych z różnych badań. Grupa ta opublikowała ostatnio nowe równanie24 o nazwie CKD-EPI, które opracowano na podstawie populacji 8 254 osób, u których GFR mierzono za pomocą klirensu iotalaminianu (średnia, 68ml/min/1,73m2, SD = 40ml/min/1,73m2), uwzględniającego takie zmienne, jak stężenie kreatyniny w surowicy, wiek, płeć i grupa etniczna. Równanie to ma różne wersje w zależności od grupy etnicznej, płci i wartości kreatyniny (Tabela 1). Według tego samego badania, porównanie CKD-EPI z MDRD-IDMS wskazuje, że to pierwsze daje lepsze wyniki, szczególnie dla wartości GFR powyżej 60ml/min/1,73m2. Porównanie z bezpośrednim pomiarem GFR wykazuje, że jest on dokładniejszy i bardziej precyzyjny, dlatego autorzy doszli do wniosku, że CKD-EPI może zastąpić MDRD-IDMS w codziennej praktyce klinicznej. Celem niniejszej pracy jest porównanie szacunkowych wartości GFR uzyskanych za pomocą nowego równania CKD-EPI z wartościami pochodzącymi z MDRD-IMDS w dużej kohorcie pacjentów oraz analiza wpływu nowego równania na klasyfikację populacji do różnych stadiów CKD w zależności od GFR.
MATERIAŁ I METODY
Pacjenci
Wykorzystano dane z kohorty 28 123 pacjentów (8 406 kobiet i 19 717 mężczyzn) w wieku od 18 do 97 lat, u których oznaczono stężenie kreatyniny w surowicy w celu oceny funkcji nerek. Pomiary miały miejsce w laboratorium Fundacji Puigvert między styczniem 2006 a majem 2009 roku. Fundacja Puigvert jest ośrodkiem referencyjnym specjalizującym się w urologii, nefrologii i andrologii. Mieści się w Szpitalu Uniwersyteckim Santa Creu i Sant Pau w Barcelonie i obsługuje populację liczącą około 450 000 mieszkańców w obszarze metropolitalnym Barcelony. Wszystkim wynikom oznaczeń kreatyniny towarzyszy szacunkowy GFR obliczony metodą MDRD-IDMS, a także komentarz kliniczny dotyczący stadium CKD, które jest przypisywane w zależności od wartości GFR zgodnie z zaleceniami zawartymi w dokumencie Consensus Document on estimating glomerular filtration rate opracowanym przez SEQC i SEN.14 Do grupy badanej z GFR wyższym niż 60ml/min/1,73m2 włączono jedynie przypadki prezentujące patologiczny białkomocz na podstawie całkowitej eliminacji białek z moczem w ciągu 24 godzin, stosunku białka do kreatyniny lub albuminy do kreatyniny w porannej próbce moczu lub obecności białek na pasku testowym w losowo wybranej próbce moczu. Ostateczna kohorta pacjentów włączonych do badania liczyła 14 427 osób: 5 234 kobiet i 9 193 mężczyzn. Kryteria doboru pacjentów i włączenia do badania przedstawiono na rycinie 1. U niektórych pacjentów czynność nerek oceniano kilkakrotnie, dlatego całkowita liczba pomiarów uwzględnionych w badaniu wynosi 51 579.
Metody
Określenie stężenia kreatyniny w surowicy wykonano przy użyciu skompensowanego kinetycznego testu Jaffe’a (Roche Diagnostics), który oferuje wyniki identyfikowalne z metodą referencyjną IDMS. Wartości wyrażone są w μmol/l. Szacowany GFR jest obliczany przy użyciu wzorów MDRD-IDMS i CKD-EPI, a wartości są wyrażone w ml/min/1,73m2. W moczu białka całkowite oznaczane są za pomocą testu turbidymetrycznego z chlorkiem benzetonium. Albumina jest oznaczana metodą immunoturbidymetryczną z użyciem przeciwciał poliklonalnych, a kreatynina metodą kinetyczną Jaffe. Wszystkie oznaczenia do listopada 2007 r. wykonano przy użyciu analizatora chemicznego Cobas Integra 700® (Roche Diagnostics), a kolejne badania przy użyciu analizatora Cobas 6000® (Roche Diagnostics). Ocenę białkomoczu z paska testowego przeprowadzono przy użyciu systemu Combur Test® M z automatycznym odczytem podawanym przez aparat do badania moczu Miditron M® (Roche Diagnostics); do badania włączono tylko tych pacjentów, u których stwierdzono białkomocz > 2+, odpowiadający stężeniu 0,75g/l. Wszystkie ilości biologiczne użyte w tym badaniu zostały poddane wewnętrznym i zewnętrznym programom kontroli jakości i wszystkie przekroczyły specyfikacje jakości analitycznej zalecane dla ich poszczególnych przypadków.
Analiza statystyczna
Obliczyliśmy średnią i odchylenie standardowe dla wartości wieku, kreatyniny i GFR oszacowanych wg MDRD-IDMS (FGMDRD-IDMS) oraz wg CKD-EPI (FGCKD-EPI) dla całej badanej populacji oraz dla grup populacyjnych z podziałem na płeć. Populację podzielono na stadia CKD (od 1 do 5), przyjmując za wartość referencyjną GFR uzyskany wg MDRD-IDMS. Biorąc pod uwagę szeroki zakres i różne znaczenie kliniczne stadium 3 CKD, stadium to podzielono na podetapy 3A (GFR 45-59ml/min/1,73m2) i 3B (30-44ml/min/1,73m2), zgodnie z zaleceniami niektórych towarzystw medycznych.16,19 Obliczono średnią i odchylenie standardowe GFR uzyskanego dla każdego stadium za pomocą MDRD-IDMS i CKD-EPI. Wykorzystując proces statystyczny Blanda-Altmana,25 obliczyliśmy różnice między wartościami GFR przypisanymi dla każdego ze wzorów. Zostały one wyrażone jako wartości bezwzględne (FGMDRD-IDMS – FGCKD-EPI, ml/min/1,73m2) oraz jako procent różnic ( X 100, %). Wreszcie, oceniliśmy procent zgodności między stadiami CKD przypisanymi według każdej z formuł; w przypadku rozbieżności oceniliśmy, jak CKD-EPI przeklasyfikował badanych. Wszystkie analizy przeprowadzono przy użyciu programów SPSS Statistical Analysis® (wersja 17.0) i MedCalc® (MedCalc Software, wersja 8.1.0.0).
WYNIKI
W tabeli 2 przedstawiono charakterystykę demograficzną badanej populacji oraz wartości stężenia kreatyniny w surowicy i GFR oszacowane według każdego ze wzorów dla całej grupy badanej i grup z podziałem na płeć. Wartości współczynnika filtracji kłębuszkowej były istotnie różniące się (p 2 wyższe przy zastosowaniu metody CKD-EPI w grupie ogólnej, wyższe o 1,9ml/min/1,73m2 u kobiet i niższe o 0,2ml/min/1,73m2 u mężczyzn. Wyniki zgodności dla obu wzorów, odnoszące się do osób, które zostały zakwalifikowane do tego samego stadium CKD obiema metodami, przy czym jako odniesienie przyjęto stadium przypisane metodą MDRD-IDMS, w ocenie całej populacji wahały się od 79,4% dla stadium 3A CKD do 98,6% dla stadium 5 CKD (tab. 3). W przypadku podziału grupy ze względu na płeć zaobserwowano wyższą zgodność dla grupy mężczyzn, z zakresem od 81,7% dla stadium 3A CKD do 99,2% dla stadium 5 CKD, a niższą dla grupy kobiet. Tylko 74,3% i 76,0% pacjentów w stadiach CKD odpowiednio 3A i 2 zostało przypisanych do tego samego stadium przez oba równania. Biorąc pod uwagę dużą liczbę pacjentów w podeszłym wieku (42,2% miało więcej niż 70 lat), oceniliśmy wagę zmiennej wieku w nowym równaniu i zaobserwowaliśmy niższy poziom zgodności między dwoma równaniami dla pacjentów poniżej 70. roku życia. Największe różnice między oboma równaniami można było zaobserwować, gdy zmienne płci i wieku były uwzględniane jednocześnie. W tabeli 4 przedstawiono liczbę i odsetek przypadków ze zgodnym przypisaniem stopnia zaawansowania dla obu równań (pogrubienie, w kolorze czarnym) oraz reklasyfikację przypisaną przez CKDEPI dla przypadków niezgodnych. W przypadku CKD w stadium 4 i 5 poziom zgodności wynosił odpowiednio powyżej 87% i 95% dla wszystkich przypadków, niezależnie od wieku i płci. Dla stadium 3B CKD największe rozbieżności stwierdzono w grupie kobiet poniżej 70. roku życia; 24,7% przypadków zostało przeklasyfikowanych do stadium 3A CKD przez CKD-EPI. W przypadku osób w stadium 3A nowe równanie poprawiło stopień zaawansowania CKD w grupie poniżej 70. roku życia niezależnie od płci. Dla stadiów z GFR powyżej 60ml/min/1,73m2 skuteczność CKD-EPI w porównaniu z MDRD-IDMS była zróżnicowana. Odnotowano, że ponad 40% badanych w wieku powyżej 70 lat zostało przesuniętych ze stadium 1 CKD do stadium 2 CKD. W tabeli 5 przedstawiono wartości stężenia kreatyniny w surowicy i GFR wyznaczone przez oba równania dla różnych stadiów CKD, a także wyniki analizy Blanda-Altmana. Są one wyrażone jako wartości bezwzględne różnic (ml/min/1,73m2) oraz jako odsetki, dla populacji ogółem i dla grup z podziałem na płeć. Wartość dodatnia wskazuje, że wartości GFR uzyskane z CKD-EPI są przeszacowane w porównaniu z wartościami z MDRD-IDMS i odwrotnie. Ogólnie rzecz biorąc, nowe równanie pozwoliło uzyskać wartości GFR nieco niższe dla 4-5 stadium CKD, a wyższe dla pozostałych stadiów. Analiza według płci wykazała, że CKD-EPI generuje wyższe wartości GFR we wszystkich stadiach (z wyjątkiem stadium 5 CKD). Zwracamy uwagę na wzrost wartości GFR o 8,5% i 9,2% odpowiednio dla stadiów 2 i 3 CKD w grupie kobiet.
DISCUSSION
Publikacja w 2002 roku wytycznych Kidney Disease Outcomes Quality Initiative (K/DOQI)16 National Kidney Foundation stworzyła podstawy do definiowania i klasyfikowania stadiów CKD. Zgodnie z kryteriami K/DOQI, CKD jest rozumiana jako: Obecność GFR poniżej 60ml/min/1,73m2 w okresie czasu większym lub równym trzem miesiącom. Obecność uszkodzenia nerek, z lub bez obniżenia GFR w okresie większym lub równym trzem miesiącom, wykazanego bezpośrednio przez nieprawidłowości histologiczne w biopsji nerki lub pośrednio przez obecność albuminurii, białkomoczu, nieprawidłowego osadu moczu lub nieprawidłowych badań obrazowych. Kombinacja obu kryteriów diagnostycznych jest podstawą klasyfikacji CKD w 5 stadiach. Należy pamiętać, że w początkowych stadiach (1 i 2) sama wartość GFR nie jest markerem diagnostycznym; musi być obecny marker związany z uszkodzeniem nerek. Obecnie w różnych przewodnikach praktyki klinicznej w CKD zaleca się ocenę GFR za pomocą równań opartych na pomiarach kreatyniny i różnych zmiennych, takich jak wiek, płeć czy grupa etniczna. Chociaż opublikowano wiele równań służących do tego celu, obecnie najbardziej akceptowanym jest MDRD. Zastosowanie równania MDRD doprowadziło do znacznego postępu we wczesnym rozpoznawaniu CKD. Fakt ten wiąże się z istotnymi korzyściami, ponieważ wczesne rozpoznanie pozwala na rozpoczęcie różnych terapii mających na celu zatrzymanie lub spowolnienie postępu choroby nerek oraz leczenie jej powikłań (niedokrwistość, wtórna nadczynność przytarczyc itp.), gdy są one we wczesnym stadium. Ostatecznym celem jest poprawa jakości opieki i przeżywalności pacjentów.26-28 Równanie MDRD ma jednak szereg ograniczeń wynikających z populacji wykorzystanej do opracowania tego pomiaru,12 która składała się głównie z osób o różnym stopniu zaawansowania CKD (średnia GFR 40ml/min/1,73m2). Wyróżnia się brak precyzji i systemowe niedoszacowanie29-34 , szczególnie dla wartości GFR powyżej 90ml/min/1,73m2. Niedoszacowanie może spowodować, że niektóre osoby będą poddawane niepotrzebnym badaniom, otrzymają zbyt małe dawki leków wydalanych przez nerki, zostaną odsunięte od diagnostyki obrazowej wymagającej użycia kontrastu oraz otrzymają bardziej agresywne leczenie w celu obniżenia czynników ryzyka sercowo-naczyniowego. Jednocześnie prawie nieistniejąca reprezentacja grup etnicznych innych niż czarna lub biała w populacji, w której opracowano wzór, stała się powodem opublikowania równań z określonymi współczynnikami korygującymi dla innych grup etnicznych.35,36 Z tego samego powodu opowiadamy się za potrzebą poszukiwania nowych markerów funkcji nerek lub nowych równań do szacowania GFR, które dawałyby lepsze wyniki niż MDRD, zwłaszcza dla GFR powyżej 60 ml/min/1,73m2. Cystatyna C jest endogennym markerem filtracji kłębuszkowej, który został zaproponowany jako alternatywa dla kreatyniny i wzorów szacowania GFR do oceny funkcji nerek. W ostatnich latach opublikowano wiele badań porównujących potencjał cystatyny C jako markera GFR z potencjałem kreatyniny. Większość z nich (ale nie wszystkie) stwierdza, że cystatyna C jest lepszym markerem. Dostępne są jednak różne wzory, opracowane w różnych populacjach, służące do szacowania GFR na podstawie cystatyny. Porównanie tych równań z MDRD-4 lub MDRD-IDMS daje niejednorodne wyniki.37-41 Obecnie, niezależnie od oczekiwań, że cystatyna C może być dobrym markerem GFR, zwłaszcza dla dużych wartości, żaden przewodnik praktyki klinicznej nie wymienia jej stosowania jako parametru CKD. Ostatnio CKD-EPI opublikowało nowy wzór opracowany na podstawie grupy 8 254 uczestników 10 badań klinicznych, które obejmowały chorych o różnej charakterystyce klinicznej, z chorobą nerek i bez niej oraz z szerokim zakresem wartości GFR.24 U wszystkich osób włączonych do populacji, z której uzyskano nowy wzór, wykonano pomiar GFR za pomocą klirensu iotalamidu (średnio 68 ml/min/1,72m2, SD = 40 ml/min/1,73m2), a wartości kreatyniny w surowicy (średnio 145 μmol/l) przekalibrowano zgodnie z metodą enzymatyczną firmy Roche, która zapewnia identyfikowalność z metodą referencyjną IDMS. Średni wiek populacji wynosił 47 lat, z niską reprezentacją starszych pacjentów; 9% badanych było w wieku od 66 do 70 lat, a tylko 3% było starszych niż 71 lat. Wzór uzyskano na podstawie modelu regresji liniowej do szacowania logarytmu GFR na podstawie uzyskanych wartości stężenia kreatyniny z uwzględnieniem zmiennych: wiek, płeć i grupa etniczna. Dla różnych grup etnicznych istnieją różne wersje wzoru, a w obrębie tych grup istnieją różne wzory w zależności od płci i stężenia kreatyniny (tab. 1). Wzór CKD-EPI został następnie zwalidowany w niezależnej grupie populacyjnej obejmującej 3 896 osób pochodzących z 16 badań. Porównując nową formułę z MDRD-IDMS, wyraźnie widać, że CKD-EPI daje lepsze wyniki, zwłaszcza dla wysokich wartości GFR. Jednocześnie jest on równie dokładny jak MDRD-IDMS dla wartości GFR poniżej 60ml/min/1,73m2 z mniejszym odchyleniem (mediana różnicy między zmierzonym a oszacowanym GFR 2,5ml/min/1,73m2 vs 5,5ml/min/1.73m2), lepszą precyzją (zakres międzykwartylowy między różnicami = 16,6 ml/min/1,73m2 vs 18,3 ml/min/1,73m2) i większą dokładnością (odsetek szacowanych GFR w zakresie 30% lub mniejszym od zmierzonego GFR = 84,1% vs 80,6%). Zastosowanie CKD-EPI w badaniu NHANES (1999-2006) wykazało, że mediana szacowanego GFR wynosiła 94,5 ml/min/1,73m2 w porównaniu z 85,0 szacowanym przy użyciu MDRD-IDMS, co spowodowało, że częstość występowania CKD wynosiła 11,5%, a nie 13,1%; ten spadek częstości występowania był zasadniczo spowodowany zmniejszeniem liczby przypadków klasyfikowanych jako stadium 3 CKD przez MDRD-IDMS. Z drugiej strony, reklasyfikacja pacjentów według CKD-EPI zwiększyła częstość występowania stadium 1 CKD, zmniejszając jednocześnie częstość występowania stadium 2 i 3 CKD. Rozpowszechnienie nowych wzorów oceny GFR oznacza konieczność ich walidacji w populacjach o różnej charakterystyce klinicznej. Celem naszego badania było zebranie znaczącej liczby pacjentów z szerokim zakresem wartości GFR, aby porównać wyniki GFR uzyskane przy użyciu formuły MDRD-IDMS i nowej formuły CKD-EPI oraz przeanalizować, jak wpłynęło to na klasyfikację stadium CKD. Nasze wyniki wskazują, że nowa formuła dostarcza wyższych wartości niż MDRD-IDMS. Ten wzrost GFR wiąże się z przeklasyfikowaniem pacjentów do łagodniejszych stadiów CKD; w tym celu 9,8% przypadków, które zostały sklasyfikowane jako 3B CKD, stało się 3A, 17% przypadków 3A CKD stało się stadium 2 CKD, a 15,7% przeszło ze stadium 2 do stadium 1 CKD. Ponadto analiza w podgrupach wiekowych wykazała, że ta tendencja do łagodniejszych stadiów CKD była większa w grupie osób poniżej 70. roku życia; 18,9% badanych przeszło ze stadium 3B CKD do stadium 3A, 34,1% ze stadium 3A do 2, a 24,0% ze stadium 2 do 1 CKD. Mimo że tylko 3,7% osób uwzględnionych w opracowaniu formuły CKD-EPI było w wieku powyżej 70 lat, odsetek zgodności obserwowany dla tej grupy w naszym badaniu przekracza 90% dla stadiów CKD od 2 do 5; jednak wśród osób zaliczonych do stadium 1 CKD według MDRDIDMS duża liczba przypadków została zakwalifikowana do stadium 2 CKD według formuły CKD-EPI. Uważamy, że takie przesunięcie do stadium o niższym GFR wynika z uzyskania przez formułę MDRD-IDMS zbyt wysokich wartości GFR dla niektórych osób w tej populacji. Wartości te są trudne do uwierzenia, biorąc pod uwagę związane z wiekiem fizjologiczne obniżenie GFR, a wynikają z niskich stężeń kreatyniny w surowicy, jakie występują u wielu z tych chorych. Wzór CKD-EPI jest dostępny w różnych wersjach w zależności od poziomu kreatyniny, jak widzimy w tabeli 1. Ma to na celu lepsze dopasowanie wyników do prawdziwej wartości GFR uzyskanej poprzez pomiar klirensu iotalaminy. Najważniejszym aspektem tego badania jest to, że jest to pierwsza publikacja próbująca zwalidować nową formułę CKD-EPI w naszej społeczności, a także to, że została ona przeprowadzona w dużej kohorcie pacjentów. Musimy jednak pamiętać, że nie znamy prawdziwej wartości GFR, ponieważ nie mamy możliwości jej bezpośredniego pomiaru metodą referencyjną. Jednak to wstępne zadanie zostało już wykonane w oryginalnej publikacji, dlatego uważamy, że wyniki są w dużej mierze porównywalne. Nasze wyniki pokrywają się z wynikami uzyskanymi przez Levey’a pod tym względem, że pacjenci zostali ponownie przypisani do łagodniejszych stadiów CKD, co jest szczególnie prawdziwe w grupie sklasyfikowanej jako stadium 3 CKD według MDRD-IDMS. Wyniki te wynikają z charakterystyki populacji, na podstawie której opracowano wzór CKD-EPI (osoby o średnim poziomie GFR 68 ml/min/1,73m2, w porównaniu z 40 ml/min/1,73m2 w grupie wykorzystanej do opracowania wzoru MDRD), a także z zastosowania metod standaryzowanych w porównaniu z metodą referencyjną pomiaru kreatyniny w surowicy. W przewodnikach praktyki klinicznej, które zostały ostatnio opracowane przez SEN wspólnie z Hiszpańskim Towarzystwem Medycyny Rodzinnej i Społecznej (semFYC)42 , stwierdzono, że skierowanie do nefrologa jest zalecane u pacjentów poniżej 70. roku życia z GFR poniżej 45ml/min/1,73m2. Nasze wyniki wskazują, że duża liczba pacjentów, którzy są obecnie uważani za kandydatów do skierowania, nie byłaby już nimi. Miałoby to istotne konsekwencje dla zdrowia społecznego, ponieważ pomogłoby zmniejszyć zatłoczenie na oddziałach nefrologicznych. Tymczasem możemy kontynuować prace nad poprawą dokładności i precyzji metod pomiaru i szacowania GFR. Ponadto uważamy, że kolejnym ważnym czynnikiem, który należy rozważyć przy ocenie nowych wzorów szacunkowego GFR, jest ocena ich potencjału jako czynników prognostycznych dla chorób układu sercowo-naczyniowego i/lub przeżycia.
Podziękowania
To badanie zostało przeprowadzone przy wsparciu Hiszpańskiej Sieci Badań Nefrologicznych (REDinREN) 16/06. RETICS. Instytut Badań nad Zdrowiem Carlos III. Madrid, Spain.

Tabela 1. Szacowany współczynnik filtracji kłębuszkowej wzór CKD-EPI
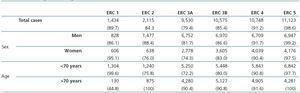
Tabela 2. Charakterystyka demograficzna populacji w podziale na płeć i wiek, z podziałem na grupy wiekowe
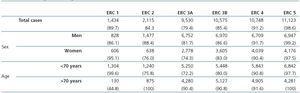
Tabela 3. Zgodność w klasyfikacjach stadium CKD dla szacowanych współczynników filtracji kłębuszkowej (GFR) z zastosowaniem wzorów MDRDIDMS i CKD-EPI

Tabela 4. Zgodności (zaznaczone pogrubioną czarną czcionką) w klasyfikacji stadiów przewlekłej choroby nerek (CKD) dla współczynnika filtracji kłębuszkowej (GFR) oszacowanego za pomocą wzorów MDRD-IDMS i CKD-EPI, przyjmując GFR wg MDRD-IDMS jako odniesienie oraz uwzględniając płeć i

Tabela 5. Wartości stężenia kreatyniny w surowicy i współczynnika filtracji kłębuszkowej oszacowane za pomocą wzorów MDRD-IDMS (GFRMDRD-IDMS) i CKDEPI (GFRCKD-EPI) dla różnych stadiów przewlekłej choroby nerek (CKD) oraz analiza zgodności wzorów GFRCKD-EPI i GFRMDRD-IDMS z wykorzystaniem wzorów
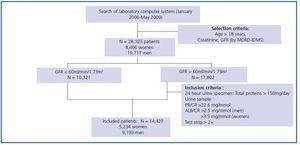
Rycina 1.