Molecules in tissue are not fixed in place but move around over time. Parte deste movimento está relacionado com processos activos tais como a circulação de sangue, enquanto outro movimento é simplesmente um movimento aleatório sem objectivo líquido. Este último fenómeno está relacionado com o calor (energia) no tecido e é referido como movimento Browniano. Como referido, não há nenhuma direcção de fluxo da rede – as moléculas simplesmente agitam e ricocheteiam em solução, movendo alonga ao acaso, mudando de direcção à medida que chocam com outras moléculas. O movimento das moléculas ao longo do tempo é referido como difusão molecular.
O movimento destas moléculas de água pode ser restringido pela presença de barreiras, principalmente membranas celulares. Pode ver uma ilustração deste processo abaixo. O grau de restrição de difusão pode ser quantificado por um coeficiente de difusão, que reflecte a distância média que uma partícula irá mover num segundo; o coeficiente de difusão real não é geralmente importante, mas é útil para a terminologia.
| Free Water | Intracellular Water |
| Seu navegador não suporta a tela HTML. | |
Ilustração do movimento browniano; esquerda, difusão livre de água e direita, movimento restringido por uma membrana celular. Executar os tempos de simulação -several para ver como os caminhos são restringidos pela célula. A linha vermelha marca o caminho da molécula, enquanto a linha cinzenta mostra o deslocamento líquido no final da corrida.
Como pode imaginar, alterações na densidade celular do tecido e a quantidade de água intracelular versus extracelular terão impacto no grau de restrição de difusão dentro desse volume de tecido. Condições tais como infartos isquémicos dentro do cérebro, abcessos piogénicos, e pequenos tumores de células azuis redondas tendem a produzir uma difusão altamente restrita; cistos e edema produzem baixos graus de restrição de difusão.
Imagem ponderada pela difusão
Gradientes de difusão. Como temos salientado, a difusão pode variar com base numa patologia subjacente; a capacidade de medir e comparar os coeficientes de difusão dentro de um órgão é importante para um número crescente de aplicações, tais como a avaliação para o AVC agudo. Uma sequência de impulsos MR pode ser concebida para ser sensível à difusão de moléculas, utilizando conceitos semelhantes aos responsáveis pela desfatização relacionada com o fluxo e o MRA de contraste de fase. Em particular, as partículas que se movem entre a aplicação de dois impulsos de gradiente espacial experimentarão forças de gradiente diferentes (uma vez que estão em posições diferentes).
Rembrar que a aplicação de um impulso de gradiente induz um deslocamento de fase na precessão do próton; para rever este conceito, pode ler a secção codificação onphase- para localização espacial. Se aplicarmos um gradiente e depois o invertermos exactamente, as partículas que se encontram na localização por amostragem não sofrerão um deslocamento de fase líquido, enquanto que as partículas que se moveram acabarão com um deslocamento de fase.
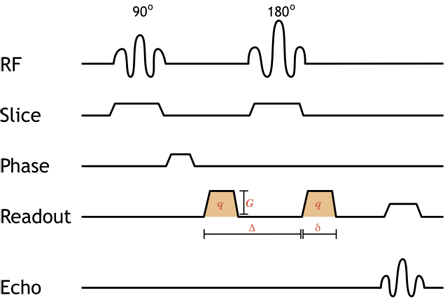
Diagrama de pulso simplificado de uma sequência de imagem ponderada por difusão de spin-echo. Os gradientes laranja sombreados são os gradientes de difusão (note-se que ambos são positivos uma vez que o pulso de 180 graus entre eles inverte a direcção da precessão, pelo que o segundo é realmente negativo). A adição de gradientes de difusão iguais e emparelhados à sequência padrão de spin-echo faz com que os prótons em movimento se desfaçam. O grau de ponderação da difusão depende da força do gradiente (amplitude G e duração δ), bem como do intervalo de tempo entre eles (Δ) – isto é referido como o valor b,discutido abaixo.
br>>p>p>Seu navegador não suporta a tela HTML.br>
br>>>p>Illustração dos gradientes usados para a imagem ponderada pela difusão. Na metade superior da imagem, estão representados dois protões estacionários cinzentos; na metade inferior estão representados dois protões móveis azuis. O gradiente de difusão (que varia ao longo do eixo x) é mostrado na parte inferior em vermelho quando está ligado. O painel direito mostra a fase líquida do ‘voxel’ contendo ambos os prótons; o comprimento da linha diminui à medida que os prótons se desfazem.Para os prótons estacionários, notar que estão sincronizados no início da sequência de impulsos, desfase com o gradiente, e depois refase à medida que o gradiente se inverte. Contudo, os prótons móveis não podem refazer a fase desde que se moveram – não experimentarão a mesma força de gradiente que inicialmente. Estes prótons acumulam mudanças de fase desiguais, e o sinal líquido é diminuído (desfasamento).
b valor. Para uma imagem ponderada pela difusão, podemos alterar a quantidade de peso DWI que queremos, ou seja, qual é o nosso ‘limiar’ de restrição de difusão.Ao ajustar o espaçamento temporal e a força dos gradientes de difusão, podemos tornar a imagem mais ou menos sensível ao movimento molecular. Fazendo o gradiente ou aumentando o tempo entre os gradientes de desfasamento e de refase provocará muito mais desfasamento a partir da mesma quantidade de movimento Browniano. O grau de ponderação da DWI é referido como o valor b (quantitativamente, b ∝ q2 * Δ , onde q é a força do gradiente e Δ é o tempo entre os dois gradientes). As imagens de baixo valor b são apenas ligeiramente afectadas pelas propriedades de difusão dos tecidos. Um valor b mais elevado dará uma imagem globalmente mais escura, uma vez que a maioria dos tecidos perderá sinal do movimento molecular – mas as lesões restritas serão mais conspícuas; tipicamente, adquiriremos múltiplos valores b por razões discutidas abaixo para calcular uma imagem ADC. Ver abaixo uma simulação ilustrando este ponto.
DWI Pulse Sequence. Podemos agora discutir detalhes práticos – como é que se adquire uma imagem ponderada por difusão? As sequências típicas de DWI são sequências de spin echosequences, com impulsos de 90 e 180 graus. (Estão a ser desenvolvidas novas formas de executar DWI, nem todas utilizam sequências de eco de spin). Os diffusiongradients são ligados antes e depois do impulso de 180 graus (são ambos gradientes positivos porque o impulso de 180 graus serve para inverter o efeito do segundo impulso). As sequências DWI precisam de ser extremamente rápidas a fim de eliminar qualquer movimento dentro da parte do corpo – uma vez que todo o propósito da sequência DWI é medir movimentos infinitesimais das moléculas de água, as nossas imagens serão completamente destruídas por movimentos macroscópicos. Durante muito tempo,a sequência mais rápida disponível foi a imagem eco-planar (EPI), e praticamente todas as sequências DWI actualmente utilizadas usam EPI.
Idealmente, gostaríamos que as nossas imagens DWI fossem inteiramente ‘ponderadas DWI’ – por outras palavras, veríamos apenas os resultados da difusão, e não outras propriedades do tecido. O TR é longo para reduzir os efeitos T1 e melhorar o sinal. O TE é mantido o mais curto possível, mas a inserção do gradiente de difusão após o pulso de 180 requer um TE mais longo; portanto, as imagens DWI são também T2 ponderadas. Este é um ponto muito importante a ter em conta – as lesões podem ser brilhantes no DWI apenas com efeitos T2 (isto é conhecido como brilho T2), e as lesões com difusão restrita e relaxamento T2 longo willappear muito brilhante!
Fat. A gordura cria problemas no DWI por várias razões. Primeiro, é brilhante nas imagens DWI porque as moléculas de gordura não se movem muito (são arelativamente restritas); o sinal de gordura pode obscurecer as lesões. Em segundo lugar, o artefacto de deslocamento químico (do primeiro tipo) é muchexagerado pela imagem eco-planar (EPI), muitas vezes cerca de 10 pixels de um deslocamento! (Isto porque os turnos de fase se acumulam ao longo de um único disparo da sequência EPI; para uma discussão técnica, ver as referências). Assim, a gordura dos tecidos subcutâneos pode obscurecer lesões no cérebro ou no fígado. Por estas razões, a supressão de gordura homogénea é necessária para as imagens DWI.
Coeficiente de Difusão Aparente
Como discutido acima, as imagens DWI são inerentemente ponderadas em T2. Portanto, as lesões com um longo relaxamento T2 parecerão brilhantes, mesmo que não restrinjam a difusão. Este efeito será particularmente visível em imagens de baixo valor b, onde o peso de difusão é menor (ou seja, as lesões com difusão rápida não perderam muito sinal e por isso continuarão a ser brilhantes). Devido ao seu extremamente longo T2, a água livre (por exemplo, CSF, quistos) será brilhante mesmo em imagens de valor b relativamente elevado. Gostaríamos de eliminar os efeitos T2 para obter uma ideia mais precisa da restrição da difusão e eliminar pontos brilhantes espúrios. Para tudo isto, podemos efectivamente calcular o coeficiente de difusão utilizando várias séries DWI com diferentes valores b.
Coeficiente de Difusão Parente. Os coeficientes de difusão que medimos com a RM representam médias de todo o voxel e de cada direcção de difusão (ver discussão sobre anisotropia e DTI mais tarde). Por conseguinte, utilizamos a palavra aparente para descrever os valores que calculamos. O sinal de um determinado tecido diminui exponencialmente com o aumento do valor b. Dado um coeficiente de difusão aparente D, a intensidade do sinal Iis
I = I0 * e-b * D, onde I0 depende das características T2
Se adquirirmos pelo menos 2 sequências DWI com diferentes valores b, podemos ligá-las à equação para resolver para D. Tipicamente, são usados pelo menos 3 valores b diferentes para melhorar o ruído (e.g. 40, 400, e 800); podemos pegar no registo da intensidade para linearizar o gráfico e depois usar a regressão linear para geta best-fit D. Ao plotar D para cada pixel, obtemos a imagem ADC (por vezes chamada mapa ADC).
|
DWI b-value: |
ADC |
|
| Seu navegador não suporta a Tela HTML. | Seu navegador não suporta a Tela HTML. | Seu navegador não suporta a Tela HTML. |
Simulação de como diferentes valores b afectam a aparência das imagens DWI e como calcular o ADC. Imagens DWI à esquerda, simuladas, mostrando um CSF brilhante nas imagens de baixo valor b e uma maior visibilidade do traço frontal esquerdo nas imagens de alto valor b. Centro, gráfico do telog da intensidade do sinal dos diferentes tecidos (azul, CSF; cinzento, cérebro; castanho, AVC) com valores b variáveis. A inclinação da linha de ligação do ponto é o ADC. direita, imagem simulada do ADC; áreas de restrição de difusão, que têm a inclinação mais plana na trama central, têm o sinal mais escuro na imagem do ADC.
As áreas de restrição de difusão perderão o menor sinal nas imagens de alto valor b (porque os seus prótons não se estão a mover). A inclinação da linha no gráfico DWI (ver acima) será plana, e portanto o valor do ADC será pequeno (portanto, pixels escuros). Por outro lado, as áreas de difusão rápida perderão o sinal de menor valor à medida que os valores b aumentam, dando uma grande inclinação – e pixels brilhantes na imagem do ADC. É importante notar que o brilho T2 – ou seja, a luminosidade das imagens onDWI relacionadas com o sinal T2 subjacente no tecido apenas afecta a posição inicial dos pontos no gráfico DWI; não afecta a inclinação,portanto a imagem ADC é independente do brilho T2 – reflecte apenas a difusão.
Clinicamente, normalmente ainda usamos imagens DWI porque as anomalias brilhantes são muito mais fáceis de ver do que as anomalias escuras (pode reparar nisto na simulação acima). As pessoas desenvolveram várias estratégias para transformar a imagem do ADC num mapa “brilhante = mau”; por exemplo, o mapa exponencial do ADC (EADC) toma o exponencial dos valores do ADC, levando a uma escala invertida mais semelhante à do DWI (mas mais uma vez, eliminando os efeitos de brilho T2). Outra razão importante para utilizar imagens DWI é que, uma vez que a imagem do ADC depende de várias imagens DWI, é inerentemente mais susceptível a artefactos do que as imagens individuais DWI. Finalmente, para muitas anomalias, elas não só restringem a difusão como são brilhantes em T2; assim, podemos realmente tirar partido do efeito de brilho T2 para tornar as lesões mais evidentes, e depois confirmar a verdadeira restrição de difusão no mapa ADC.
Diffusion Tensor Imaging
Até agora, tivemos uma visão simplista da difusão – que as moléculas de água podem difundir-se em todas as direcções igualmente. Na verdade, pelo menos em alguns tecidos, isto não é de todo verdade. Nos tecidos altamente estruturados, particularmente nos nervos e nas vias de matéria branca no cérebro, a difusão ocorre preferencialmente numa direcção. Na matéria branca, as bainhas de mielina circundam os neurónios e impedem a difusão de água através da bainha, mas permitem-na ao longo da direcção dos axónios. A difusão que depende da direcção é referida como anisotrópica (ou seja, não é igual em todas as direcções). Isso significa que se medirmos a difusão usando gradientes numa direcção, obteríamos uma resposta diferente do que se a medíssemos noutra direcção. Igualmente importante, se medirmos a difusão numa direcção, obteremos respostas diferentes para diferentes partes da mesma matéria branca (saudável), dependendo da direcção dos axónios em cada parte.
Intuitivamente, seria lógico que a solução para este problema é medir a difusão em várias direcções e criar algum tipo de média – isto anularia qualquer viés direccional. O método mais simples para medir a difusão em diferentes direcções é chamado difusão tensorial ou DTI.DTI assume que dentro de cada voxel existe um único enviesamento direccional, por exemplo, uma única direcção do feixe neuronal. Em seguida, modela a difusão dentro de um axonnão como um escalar (número único) mas como uma elipsóide tridimensional, que é chamada tensor.

Illustração do tensor de difusão. Um feixe de axónios (amarelo) é ilustrado em 3 dimensões. As moléculas de água podem difundir os axónios mas não através deles. O tensor de difusão (castanho) representa a difusão como elipsóide, orientada ao longo dos axónios com a espessura do elipsóide em qualquer direcção correspondente ao coeficiente de difusão nessa direcção em particular. Assim, a elipse tem uma cintura fina uma vez que o tensor de difusão é baixo através dos axónios, mas a elipse é alongada uma vez que o tensor de difusão é alto ao longo do eixo dos axónios.
A partir da ilustração acima, pode-se ver que a especificação do tensor de difusão requer dois conjuntos separados de parâmetros: a direcção de difusão mais rápida (isto é, a direcção do feixe de axónios) e os coeficientes de difusão reais ao longo e através dos axónios. Uma direcção no espaço tridimensional requer 3 números; e a espessura da elipse requer 3 números (para cada eixo da própria elipse). Isto significa que o DTI requer a medição da difusão em 6 direcções diferentes. (Estas direcções precisam de ser medidas para cada valor b não nulo.)
sequências DTI são necessárias para produzir mesmo imagens regulares ponderadas por difusão no cérebro – caso contrário, as vias de matéria branca parecerão restringir a difusão. As imagens de difusão média são então produzidas através da média de três das direcções, e é isto que é tipicamente utilizado para mapas DWI e ADC. No entanto, adquirindo as 6 direcções diferentes, podemos também calcular outros mapas. Um dos mais comuns é o mapa de anisotropia fracionária (FA). Recordemos que a anisotropia representa o grau em que a difusão não é a mesma em todas as direcções; FA é calculado comparando os comprimentos de cada eixo da elipsóide do sensor com a sua média. Se houver uma grande diferença (como na ilustração acima), então o FA é elevado, representando a difusão anisotrópica. As vias normais de matéria branca têm FA elevada, que se perde em muitos processos de doença.
Tractografia. Finalmente, o DTI pode produzir boas imagens de baixa resolução de direcções gerais da matéria branca; calculando a direcção principal da elipsóide tensora, obtemos a direcção média dos feixes axonais no voxel. Podemos codificar os voxels por direcção, obtendo um mapa de tractografia. Uma tractografia muito mais sofisticada e de alta resolução pode ser obtida através da medição da difusão em mais direcções. Isto pode ter em conta áreas de cruzamento de feixes de fibras (que seriam apenas calculadas como média no DTI regular). Ao obter estes mapas, podemos criar mapas de conectividade cerebral in vivo de 3-dimensão. Esta é actualmente uma área de investigação activa.
Movimento Incoerente Intravoxel
DWI Tradicional assume que todas as moléculas de água dentro de um voxel se comportam da mesma forma (daí um único ADC por voxel). Claro que isto não é verdade: a experiência das moléculas de água em ambientes muito diferentes, mesmo dentro de um único voxel. As moléculas em sangue corrente têm uma velocidade de base e tão difusa muito rapidamente; os compartimentos intra e extracelulares também têm uma difusividade diferente. Embora o modelo simplista seja suficiente para a maioria dos fins clínicos (por exemplo, AVC), os dados emergentes sugerem que algumas descobertas clinicamente relevantes podem ser encontradas em modelos mais complexos. As duas principais categorias de modelos avançados de difusão são as imagens de difusão-curtose, não discutidas aqui, e o movimento intravoxel incoerente (IVIM).
Na nossa discussão acima sobre o ADC, assumimos que a relação entre o valor b e a intensidade do sinal é linear – por outras palavras, que existe um único valor de ADC para um voxel. Na realidade, em alguns tecidos a relação não é linear. Em particular, a queda da intensidade do sinal é muito mais acentuada a baixos valores b; isto implica que existe uma pequena subpopulação de moléculas de água de difusão muito rápida. Este fenómeno é mais perceptível no fígado, e acredita-se que esteja relacionado com o fluxo de sangue nos capilares (embora o nosso entendimento seja incompleto). A fim de medir IVIM, em vez de medirADC usando 3 valores b, precisamos de usar mais (por exemplo 8) – especialmente com valores b baixos. Actualmente, o IVIM está a ser explorado como medida para fibrose hepática.
- Hagmann P, et al. “Understanding Diffusion MR Imaging Techniques: Da Imagem de Difusão Escalar à Imagem Tensora de Difusão e Mais Além”. Radiografias 26(S1): S205.
- Dietrich O, et al. “Technical aspects of MR diffusion imaging of the body”. Eur J Radiol 76: 314.
- “Chemical Shift”: Efeitos de fase”. MRI-Questões – discussão sobre o exagero do deslocamento químico nas sequências de EPI
- se estiver interessado no original (altamente técnico!) do documento DWI: Stejskal EO e Tanner JE. “Spin Diffusion Measurements”: Spin Echoes in the Presence of a TimeDependent Field Gradient”. J Chem Phys 42 (288): 288.
Koh D, et al. “Intravoxel Incoherent Motion incoerent in Body Diffusion-Weighted MRI” (Movimento Incoerente Intravoxel em Ressonância Magnética Pesada de Difusão Corporal): Realidade e Desafios”. Am J Roentgenol 188(6): 1622.