
L’ultima versione della Tavola periodica (datata 1 dicembre 2018) include i più recenti aggiornamenti rilasciati nel giugno 2018 dalla Commissione IUPAC sulle abbondanze isotopiche e i pesi atomici (CIAAW) (vedi News correlate, rilasciato il 5 giugno 2018), e in particolare per l’argon, l’assegnazione di un intervallo per il nuovo peso atomico standard che riflette il comune verificarsi di variazioni nei pesi atomici dell’elemento nei normali materiali terrestri. Un intervallo tra parentesi quadre fornisce i limiti inferiore e superiore del peso atomico standard per quell’elemento. Per gli utenti che hanno bisogno di un valore di peso atomico per un campione non specificato senza tener conto dell’incertezza, vengono forniti i valori convenzionali. Non sono elencati valori per elementi che non hanno isotopi con un’abbondanza isotopica caratteristica nei campioni naturali terrestri. Vedi PAC per maggiori dettagli o visita la Commissione II.1 @ciaaw.org
Scaricare la versione stampabile (PDF) (formato lettera o A4) o la versione A3 (PDF) o vedere le versioni precedenti
Guarda SPECIAL Chem Int Jan 2019 – International Year of the Periodic Table (IYPT) – con contributi di Jan Reedijk, Natalia Tarasova, G.J. Leigh, Sigurd Hofmann, Eric Scerri, Juris Meija, Norman E. Holden, Tyler B. Coplen, Peter Mahaffy, Ian Mills, Roberto Marquardt, e altri.
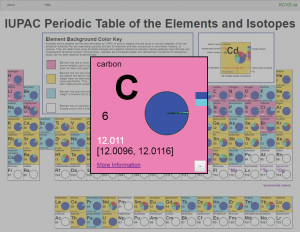 Tabella periodica degli elementi e degli isotopi IUPAC (IPTEI) per la comunità educativa
Tabella periodica degli elementi e degli isotopi IUPAC (IPTEI) per la comunità educativa
– Segui il progetto IUPAC 2007-038-3-200 e il progetto successivo 2014-024-1-200
– Leggi “Pesi atomici: No Longer Constants of Nature”, Chem Int 33(2), 10-15 (2011), http://dx.doi.org/10.1515/ci.2011.33.2.10
– Esplora la versione interattiva a https://www.isotopesmatter.com/ (o vedi il comunicato)
– Scopri di più Why Isotopes Matter! https://iupac.org/100/stories/why-isotopes-matter/
– Rivedi l’ultima revisione IPTEI elemento per elementoelemento, compresa una tabella di tutti gli isotopi stabili e radioattivi conosciuti per ogni elemento ed esempi di applicazioni pratiche di misure e tecnologie isotopiche https://iupac.org/iptei/
– Accedi a http://ciaaw.org/periodic-table-isotopes.htm una risoluzione completa di questa tabella in PDF (resa disponibile dal King’s Center for Visualization in Science).
In virtù del suo lavoro in relazione agli elementi chimici, la IUPAC può dispensare una tavola periodica aggiornata. Il coinvolgimento della IUPAC copre vari aspetti della tavola e dei dati che essa svela, e diversi rapporti e raccomandazioni, alcuni abbastanza recenti, attestano questo contributo.
In particolare, la IUPAC è direttamente coinvolta in quanto segue:
- stabilire i criteri per la scoperta di un nuovo elemento
- definire la struttura di un nome e di un simbolo temporaneo
- valutare le richieste che risultano nella convalida e nell’assegnazione di una scoperta di elemento
- coordinare la denominazione di un nuovo elemento, coinvolgendo il laboratorio di ricerca e consentendo commenti pubblici
- stabilendo regole precise su come nominare un nuovo elemento
- definendo il gruppo 1-18 e i nomi collettivi
- determinando quali elementi appartengono al gruppo 3
- rivedendo regolarmente i pesi atomici standard
La tabella è di vostro utilizzo. I dettagli sull’ultima versione sono forniti sopra. I dettagli qui sotto forniscono molteplici riferimenti alla rivista IUPAC in Pure and Applied Chemistry (PAC) e alla rivista Chemistry International (CI).
- Criteri per la scoperta di un nuovo elemento
Valutare se un elemento è stato “scoperto” non è un compito semplice. Durante la revisione dei profili di scoperta degli elementi di transfermium all’inizio degli anni 90′, IUPAC e IUPAP hanno stabilito di stabilire una serie di criteri che devono essere soddisfatti perché la scoperta di un elemento sia riconosciuta. Vedi i dettagli in PAC 1991, Vol. 63, No. 6, pp. 879-886 (https://dx.doi.org/10.1351/pac199163060879) e PAC 1993, Vol. 65, No. 8, pp. 1757-1814 (https://dx.doi.org/10.1351/pac199365081757)
Nel novembre 2018, un rapporto provvisorio ON THE DISCOVERY OF NEW ELEMENTS è stato rilasciato da IUPAC/IUPAP. Vengono presentati i criteri e le linee guida per stabilire la priorità della scoperta di potenziali nuovi elementi. – learn more
- Nome e simbolo temporanei
Mentre un elemento può essere stato rivendicato, prima che la rivendicazione sia stata convalidata e prima che l’elemento sia formalmente nominato, l’elemento ha un nome e un simbolo temporanei. Le raccomandazioni pertinenti che istituiscono questa nomenclatura sistematica sono state pubblicate nel 1978; vedi PAC 1979, Vol. 51, No. 2, pp. 381-384; https://dx.doi.org/10.1351/pac197951020381
Di conseguenza, è così che, nel marzo 2016, l’elemento 113 è stato chiamato ununtrium o con il simbolo Uut.
La storia dietro i simboli a tre lettere è raccontata in un articolo preparato da Lars Öhrström e Norman Holden e pubblicato su Chem Int 2016, Vol. 38, No. 2, pp. 4-8; https://dx.doi.org/10.1515/ci-2016-0204
- Convalida e assegnazione di una scoperta di elemento
Le rivendicazioni per le scoperte di nuovi elementi appaiono di tanto in tanto nella letteratura scientifica. La IUPAC, insieme alla IUPAP, è coinvolta nella valutazione di queste affermazioni. Di conseguenza, vengono rilasciati rapporti tecnici IUPAC che esaminano ogni riferimento pertinente e riconoscono il laboratorio o i laboratori le cui affermazioni soddisfano i criteri concordati.
Nel 2016, sono stati rilasciati due rapporti di questo tipo che riguardano gli elementi 113, 115, 117, e l’elemento 118; Vedi PAC 2016, Vol. 88, No. 1-2, pp. 139-153; https://dx.doi.org/10.1515/pac-2015-0502 e PAC 2016, Vol. 88, No. 1-2, pp. 155-160; https://dx.doi.org/10.1515/pac-2015-0501
- Nominazione nuovo elemento
Quando la scoperta di un nuovo elemento è stata validata e la priorità per la sua scoperta è stata assegnata, il processo di denominazione può iniziare. Il laboratorio a cui è stata assegnata la scoperta è invitato a proporre un nome e un simbolo. La IUPAC rivede la proposta e, se è d’accordo, dopo un’ulteriore revisione pubblica di 5 mesi, formalizza il nome. L’esempio più recente di tali raccomandazioni sono state pubblicate nel 2012 e per i nomi e i simboli degli elementi 114 e 116; Vedi PAC 2012, Vol. 84, No. 7, pp. 1669-1672; https://dx.doi.org/10.1351/PAC-REC-11-12-03
Una breve rassegna delle attuali procedure è pubblicata in un recente servizio di John Corish; Vedi CI 2016, Vol. 38, No. 2, pp. 9-11; https://dx.doi.org/10.1515/ci-2016-0205
L’8 giugno 2016, IUPAC ha rilasciato i nomi provvisori per gli ultimi 4 elementi 113, 115, 117 e 118 – vedi comunicato e il 28 novembre 2016, IUPAC ha annunciato i nomi e simboli approvati – vedi comunicato.
Per una riflessione sull’esperienza 2016 della denominazione degli elementi, vedi Chem Int Apr 2017, pp. 30-21, di Jan Reedijk; https://doi.org/10.1515/ci-2017-0222
- Come nominare un nuovo elemento
Anche qui, la IUPAC ha una serie di linee guida che delineano che tipo di nome può portare un elemento. Sia la radice che la desinenza devono essere coerenti con le raccomandazioni concordate. Le raccomandazioni dettagliate sono state pubblicate nel 2002 e una revisione pubblicata nel 2016 per accogliere meglio gli elementi del gruppo 17 e 18. Vedi PAC 2002, Vol. 74, No. 5, pp. 787-791; https://dx.doi.org/10.1351/pac200274050787 e PAC 2016, Vol. 88, No. 4, pp. 401-405 https://dx.doi.org/10.1515/pac-2015-0802 (o https://iupac.org/project/2015-031-1-200)
- Gruppo 1-18 e nomi collettivi
Dal 1988, IUPAC raccomanda che i gruppi (cioè le colonne) siano semplicemente numerati da 1 a 18. (PAC 1988, Vol. 60, No. 3, pp 431-436; https://dx.doi.org/10.1351/pac198860030431)
Lantanoidi e attinoidi sono nomi collettivi raccomandati anche dalla IUPAC. Lantanoidi (da La a Lu) è preferito rispetto al lantanide, e anche se lantanoide significa “come il lantanio” e quindi non dovrebbe includere il lantanio, il lantanio è diventato incluso dall’uso comune, tuttavia. Gli attinoidi includono da Ac a Lr.
- Gruppo 3
La questione di quali elementi debbano essere collocati esattamente nel gruppo 3 è stata discussa di tanto in tanto. Un progetto IUPAC è stato recentemente avviato per risolvere la questione. Il gruppo 3 sarà composto da Sc, Y, Lu e Lr o, sarà composto da Sc, Y, La e Ac?
Stai sintonizzato e vedi https://iupac.org/project/2015-039-2-200 e CI 2016, Vol. 38, No. 2, pp. 22-23; https://dx.doi.org/10.1515/ci-2016-0213
- Pesi atomici standard
Uno dei compiti della Commissione sulle abbondanze isotopiche e i pesi atomici (CIAAW) è quello di rivedere periodicamente le determinazioni del peso atomico. Il rapporto più recente “Atomic weights of the elements 2013” è stato pubblicato su PAC nel marzo 2016 (PAC 2016, Vol. 88, No. 3, pp. 265-291; https://dx.doi.org/10.1515/pac-2015-0305). Più recentemente, il 5 giugno 2018, la CIAAW ha raccomandato modifiche ai pesi atomici standard di 14 elementi chimici – vedi comunicato.
La Commissione è stata istituita nel 1899 (sì, nel diciotto novantanove) e ora opera sotto la Divisione Chimica Inorganica della IUPAC. (vedi www.ciaaw.org ) Rivede anche regolarmente le composizioni isotopiche degli elementi; l’ultima compilazione è anche pubblicata in PAC nel marzo 2016 (PAC 2016, Vol. 88, No. 3, pp. 293-306; https://dx.doi.org/10.1515/pac-2015-0503)