INLEIDING
Verschillende epidemiologische studies hebben aangetoond dat chronische nierziekte (CKD) een belangrijk volksgezondheidsprobleem is.1-6 De aanwezigheid ervan is in verband gebracht met een hoog risico op chronische nierziekte in het eindstadium, hart- en vaatziekten en overlijden.7 Uit gegevens van de EPIRCE-studie blijkt dat de prevalentie van CKD, die wordt beschouwd als een glomerulaire filtratiesnelheid (GFR) van minder dan 60ml/min/1,73m2 (stadia 3-5 zonder dialyse), 6,5% van de Spaanse bevolking boven de 18 jaar bedraagt.8-10 De beste index om de nierfunctie te meten is de GFR. Aangezien het meten van de inulineklaring rechtstreeks of via isotopische methoden gecompliceerd en duur is en niet in de dagelijkse praktijk kan worden gebruikt, zijn GFR-schattingen gebaseerd op vergelijkingen die gebruik maken van serumcreatinine en andere variabelen zoals leeftijd, geslacht, etnische groep en lichaamsoppervlak populair geworden.11-13 Deze vergelijkingen verbeteren de slechte correlatie die tussen creatinine en GFR blijkt te bestaan. Momenteel bevelen de meeste medische genootschappen,14-22 waaronder de Spaanse Vereniging voor Nefrologie (SEN) en de Spaanse Vereniging voor Klinische Biochemie en Moleculaire Pathologie (SEQC), het gebruik van de vergelijking van de MDRD-studie (Modification of Diet in Renal Disease) aan om de GFR te schatten; de aanbeveling verscheen in een Consensus Document over glomerulaire filtratieschattingen dat onze groep heeft helpen opstellen.14 Hierin wordt gesteld dat MDRD moet worden gebruikt op voorwaarde dat serumcreatinine wordt bepaald met hetzij de klassieke methode (MDRD-4), hetzij de verkieslijke methode MDRDIDMS, afhankelijk van de vraag of de analysemethode die wordt gebruikt om creatinine te bepalen al dan niet herleidbaar is tot de referentiemethode met behulp van isotopische verdunningsmassaspectrometrie (IDMS).15 Factoren zoals de afleidingspopulatie van de formule (patiënten met een bepaalde graad van CKD) en moeilijkheden met het gebrek aan standaardisatie voor de serumcreatininemeting (de oplossing hiervan is in een vergevorderd stadium) vormen echter een probleem voor de toepasbaarheid ervan. Het tonen van de exacte numerieke waarde voor GFR-resultaten boven 60 of 90 ml/min/1,73m2 wordt niet aanbevolen, afhankelijk van de klinische praktijkgids die u raadpleegt.14-23 Om dezelfde reden pleiten wij voor het zoeken naar nieuwe markers voor nierfunctie of nieuwe vergelijkingen voor het schatten van GFR die betere resultaten zouden geven dan de MDRD. De CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) is een onderzoeksgroep binnen het Amerikaanse National Institute of Diabetes and Digestive and Kidney Disease (NIDDK). Deze groep is opgericht om GFR-schattingsvergelijkingen te ontwikkelen en te valideren op basis van gegevens uit verschillende studies. Deze groep heeft onlangs een nieuwe vergelijking24 gepubliceerd, CKD-EPI genaamd, die is ontwikkeld op basis van een populatie van 8.254 personen bij wie de GFR is gemeten met behulp van iothalamaat klaring (gemiddelde, 68ml/min/1,73m2, SD = 40ml/min/1,73m2), waarbij rekening is gehouden met variabelen zoals serumcreatinine, leeftijd, geslacht en etnische groep. Deze vergelijking kent verschillende versies, afhankelijk van etnische groep, geslacht en creatininewaarde (tabel 1). Volgens dezelfde studie blijkt uit een vergelijking van CKD-EPI met MDRD-IDMS dat de eerste betere resultaten oplevert, vooral voor GFR-waarden boven 60 ml/min/1,73m2. Vergelijking met directe GFR-metingen toont aan dat deze nauwkeuriger en preciezer is, en daarom concluderen de auteurs dat CKD-EPI de MDRD-IDMS in de dagelijkse klinische praktijk zou kunnen vervangen. Het doel van deze studie is om de geschatte GFR waarden verkregen met behulp van de nieuwe CKD-EPI vergelijking te vergelijken met die van MDRD-IMDS in een groot patiënten cohort en het effect van de nieuwe vergelijking op de indeling van de populatie in verschillende CKD stadia te analyseren op basis van GFR.
MATERIAAL EN METHODEN
Patiënten
We gebruikten gegevens van een cohort van 28.123 patiënten (8.406 vrouwen en 19.717 mannen) tussen 18 en 97 jaar van wie het creatinineserum werd gemeten om de nierfunctie te evalueren. De metingen vonden plaats in het laboratorium van de Stichting Puigvert tussen januari 2006 en mei 2009. De Puigvert Foundation is een referentiecentrum dat gespecialiseerd is in urologie, nefrologie en andrologie. Het is gevestigd in het universitair ziekenhuis Santa Creu i Sant Pau in Barcelona, en verleent diensten aan een bevolking van ongeveer 450 000 inwoners in het grootstedelijk gebied Barcelona. Alle creatinineresultaten gaan vergezeld van een geschatte GFR, berekend volgens de MDRD-IDMS-methode, naast een klinisch commentaar over het CKD-stadium, dat wordt toegekend op basis van de GFR-waarde volgens de aanbevelingen in het Consensus Document on estimating glomerular filtration rate, opgesteld door het SEQC en de SEN.14 In de groep met een GFR hoger dan 60 ml/min/1,73m2 werden alleen gevallen opgenomen met pathologische proteïnurie op basis van de totale eliminatie van eiwitten in de urine gedurende 24 uur, de eiwit-tocreatinine- of albumine-creatinine-verhouding van de urine in een ochtendmonster, of de aanwezigheid van eiwitten op de teststrip in een willekeurig urinemonster. Het uiteindelijke cohort van patiënten in de studie omvatte 14.427 personen: 5.234 vrouwen en 9.193 mannen. De selectie- en inclusiecriteria voor de patiënten zijn weergegeven in figuur 1. Bij sommige patiënten werd de nierfunctie meermaals beoordeeld, waardoor het totale aantal in de studie opgenomen metingen op 51.579 komt.
Methode
Het bepalen van het serumcreatininegehalte gebeurde met een gecompenseerde kinetische Jaffe-test (Roche Diagnostics) die resultaten oplevert die herleidbaar zijn tot de IDMS-referentiemethode. De waarden worden uitgedrukt in μmol/l. De geschatte GFR wordt berekend met behulp van de MDRD-IDMS- en de CKD-EPI-formules, en de waarden worden uitgedrukt in ml/min/1,73m2. In de urine worden de totale eiwitten gemeten met een turbidimetrische test met benzethoniumchloride. Albumine wordt gemeten met een immunoturbidimetrische bepaling met polyklonale antilichamen, en creatinine met een kinetische Jaffe-methode. Alle bepalingen tot november 2007 zijn uitgevoerd met een Cobas Integra 700®-chemieanalysator (Roche Diagnostics), en de daaropvolgende tests met een Cobas 6000®-analysator (Roche Diagnostics). De bepaling van proteïnurie aan de hand van een teststrip werd uitgevoerd met behulp van het Combur Test® M-systeem met een automatische aflezing door een Miditron M® (Roche Diagnostics) urineanalysesysteem; alleen de patiënten met proteïnurie > 2+, overeenkomend met een concentratie van 0,75g/l, werden geïncludeerd. Alle biologische hoeveelheden die in deze studie werden gebruikt, werden onderworpen aan interne en externe kwaliteitscontroleprogramma’s, en alle overschreden de voor hun specifieke geval aanbevolen analytische kwaliteitsspecificaties.
Statistische analyse
We berekenden het gemiddelde en de standaardafwijking voor de waarden leeftijd, creatinine en GFR geschat door MDRD-IDMS (FGMDRD-IDMS) en door CKD-EPI (FGCKD-EPI) voor de gehele onderzoekspopulatie en voor de bevolkingsgroepen uitgesplitst naar geslacht. De bevolking werd ingedeeld in CKD-stadia (1 tot 5), waarbij de door de MDRD-IDMS verkregen GFR als referentiewaarde werd gebruikt. Gezien het grote bereik en de verschillende klinische betekenissen van stadium 3 CKD, werd dit stadium onderverdeeld in de substadia 3A (GFR 45-59ml/min/1.73m2) en 3B (30-44ml/min/1.73m2), zoals aanbevolen door sommige medische genootschappen.16,19 Wij berekenden het gemiddelde en de standaardafwijking van de GFR verkregen voor elk stadium met MDRD-IDMS en CKD-EPI. Met behulp van de statistische Bland-Altman methode,25 berekenden wij de verschillen tussen de GFR-waarden die voor elk van de formules waren toegekend. Deze worden uitgedrukt als absolute waarden (FGMDRD-IDMS – FGCKD-EPI, ml/min/1,73m2) en als percentage van de verschillen ( X 100, %). Ten slotte evalueerden wij het percentage concordantie tussen de CKD-stadia die volgens elk van de formules werden toegekend; in geval van discrepantie beoordeelden wij hoe CKD-EPI de proefpersonen herclassificeerde. Alle analyses werden uitgevoerd met SPSS Statistical Analysis® (versie 17.0) en MedCalc® (MedCalc Software, versie 8.1.0.0).
RESULTATEN
Tabel 2 toont de demografische kenmerken van de studiepopulatie en de verkregen waarden voor serumcreatinine en GFR geschat met behulp van elk van de formules voor de totale proefpersonengroep en de geslachtsspecifieke groepen. De waarden voor de glomerulaire filtratiesnelheid waren significant verschillend (p 2) hoger met de CKD-EPI-methode in de totale groep, 1,9ml/min/1,73m2 hoger voor vrouwen, en 0,2ml/min/1,73m2 lager voor mannen. De concordantieresultaten voor de twee formules, die betrekking hebben op personen die door beide methoden in hetzelfde CKD-stadium zijn ingedeeld met het door de MDRD-IDMS-methode toegekende stadium als referentie, varieerden bij de evaluatie van de gehele populatie tussen 79,4% voor stadium 3A CKD en 98,6% voor stadium 5 CKD (tabel 3). Bij uitsplitsing van de groep naar geslacht werd een hogere concordantie geconstateerd voor de mannelijke groep, met een bereik tussen 81,7% voor stadium 3A CKD en 99,2% voor stadium 5 CKD, en een lagere voor de vrouwelijke groep. Slechts 74,3% en 76,0% van de patiënten in CKD-stadia 3A en 2, respectievelijk, werden door beide vergelijkingen in hetzelfde stadium ingedeeld. Gezien het grote aantal oudere patiënten (42,2% was ouder dan 70), hebben wij het gewicht van de leeftijdsvariabele in de nieuwe vergelijking geëvalueerd, en een lagere mate van overeenstemming tussen de twee vergelijkingen waargenomen voor patiënten jonger dan 70. De grootste verschillen tussen beide vergelijkingen konden worden waargenomen wanneer de geslachts- en leeftijdsvariabelen tegelijkertijd werden opgenomen. Tabel 4 toont het aantal en het percentage gevallen met een concordante stadiumindeling voor beide vergelijkingen (vetgedrukt, in zwart), en de door CKDEPI toegekende herindeling voor niet-concordante gevallen. Voor stadium 4 en 5 CKD bedroeg de concordantie meer dan 87%, respectievelijk 95%, voor alle gevallen, ongeacht leeftijd of geslacht. Voor stadium 3B CKD werden de grootste discrepanties aangetroffen in de groep vrouwen jonger dan 70; 24,7% van de gevallen werd door de CKD-EPI geherclassificeerd als stadium 3A CKD. Voor personen in stadium 3A verbeterde de nieuwe vergelijking het CKD-stadium in de groep onder de 70 jaar, ongeacht het geslacht. Voor stadia met een GFR boven 60ml/min/1,73m2 was de prestatie van CKD-EPI in vergelijking met MDRD-IDMS variabel. Wij stelden vast dat meer dan 40% van de proefpersonen ouder dan 70 jaar van stadium 1 CKD naar stadium 2 CKD ging. Tabel 5 toont de serum creatinine en GFR waarden toegekend door beide vergelijkingen voor verschillende CKD stadia, evenals de Bland-Altman analyse resultaten. Zij worden uitgedrukt als absolute waarden van de verschillen (ml/min/1,73m2) en als percentages, voor de totale bevolking en voor de geslachtsspecifieke groepen. Een positieve waarde geeft aan dat GFR-waarden verkregen met CKD-EPI worden overschat in vergelijking met die van MDRD-IDMS, en vice versa. Over het geheel genomen leverde de nieuwe vergelijking GFR-waarden op die iets lager waren voor stadium 4 tot 5 CKD, en hoger voor de andere stadia. Analyse naar geslacht toonde aan dat CKD-EPI hogere GFR-waarden opleverde in alle stadia (met uitzondering van stadium 5 CKD). Wij wijzen op een toename van de GFR-waarden van 8,5% en 9,2% voor respectievelijk stadium 2 en 3 CKD in de vrouwelijke groep.
DISCUSSIE
De publicatie van de National Kidney Foundation’s Kidney Disease Outcomes Quality Initiative (K/DOQI)16 gidsen in 2002 legde de basis voor het definiëren en classificeren van CKD stadia. Volgens de K/DOQI-criteria wordt onder CKD verstaan: De aanwezigheid van een GFR lager dan 60ml/min/1,73m2 gedurende een tijdsperiode groter dan of gelijk aan drie maanden. De aanwezigheid van nierschade, met of zonder afname van de GFR gedurende een periode groter dan of gelijk aan drie maanden, direct aangetoond door histologische afwijkingen in de nierbiopsie, of indirect door de aanwezigheid van albuminurie, proteïnurie, abnormaal urinesediment of een abnormaal beeldvormend onderzoek. De combinatie van beide diagnostische criteria vormt de basis voor de indeling van CKD in 5 stadia. Opgemerkt zij dat in de eerste stadia (1 en 2) de GFR-waarde op zich geen diagnostische marker is; er moet een marker aanwezig zijn die in verband wordt gebracht met nierschade. Momenteel bevelen verschillende klinische praktijkgidsen voor CKD aan de GFR te bepalen met behulp van vergelijkingen op basis van creatininemetingen en verschillende variabelen, zoals leeftijd, geslacht of etnische groep. Hoewel er veel vergelijkingen voor dit doel zijn gepubliceerd, is de MDRD-vergelijking op dit moment de meest geaccepteerde. Het gebruik van de MDRD-vergelijking heeft geleid tot grote vooruitgang bij de vroegtijdige diagnose van CKD. Dit feit gaat gepaard met aanzienlijke voordelen, aangezien een vroegtijdige diagnose het mogelijk maakt met verschillende behandelingen te beginnen om de progressie van de nierziekte tot staan te brengen of te vertragen en de complicaties ervan (bloedarmoede, secundaire hyperparathyreoïdie, enz.) te behandelen wanneer deze zich in een vroeg stadium bevinden. Het uiteindelijke doel is de kwaliteit van de zorg en de overlevingskansen van de patiënten te verbeteren.26-28 De MDRD-vergelijking heeft echter een aantal beperkingen die voortvloeien uit de populatie die is gebruikt om die meting te ontwikkelen,12 die meestal bestond uit personen met een verschillende graad van CKD (gemiddelde GFR 40ml/min/1,73m2). Het gebrek aan precisie en de systemische onderschatting29-34 vallen op, met name voor GFR-waarden hoger dan 90ml/min/1,73m2. Onderschatting kan ertoe leiden dat sommige personen aan onnodige onderzoeken worden onderworpen, te lage doses krijgen wanneer nierafscheidende geneesmiddelen worden voorgeschreven, worden afgehouden van diagnostische beeldvormingsprocedures waarbij contrast moet worden gebruikt en agressievere behandelingen krijgen om de cardiovasculaire risicofactoren te verlagen. Tegelijkertijd heeft de bijna onbestaande vertegenwoordiging van andere etnische groepen dan zwart of blank in de populatie waarin de formule is ontwikkeld aanleiding gegeven tot de publicatie van vergelijkingen met specifieke aanpassingsfactoren voor andere etnische groepen.35,36 Om dezelfde reden pleiten wij voor de noodzaak van het zoeken naar nieuwe markers voor nierfunctie of nieuwe vergelijkingen voor het schatten van de GFR die betere resultaten zouden geven dan de MDRD, met name voor GFR’s van meer dan 60 ml/min/1,73m2. Cystatine C is een endogene glomerulaire filtratiemarker die is voorgesteld als alternatief voor creatinine en de formules voor de schatting van de GFR om de nierfunctie te beoordelen. In de afgelopen jaren zijn talrijke studies gepubliceerd waarin het potentieel van cystatine C als GFR-marker is vergeleken met dat van creatinine. In de meeste (maar niet alle) studies wordt gesteld dat cystatine C een betere marker is. Er zijn echter verschillende formules, ontwikkeld in verschillende populaties, beschikbaar voor het schatten van de GFR op basis van cystatine. Vergelijking van deze vergelijkingen met MDRD-4 of MDRD-IDMS levert heterogene resultaten op.37-41 Ongeacht de verwachtingen dat cystatine C een goede GFR-marker kan zijn, met name voor hoge waarden, vermeldt geen enkele klinische praktijkgids het gebruik ervan als CKD-parameter. Onlangs heeft de CKD-EPI een nieuwe formule gepubliceerd die is ontwikkeld met behulp van een groep van 8.254 deelnemers aan 10 klinische studies die patiënten met uiteenlopende klinische kenmerken, met en zonder nierziekte en met een breed scala van GFR-waarden omvatte.24 Bij alle personen die deel uitmaakten van de populatie waaruit de nieuwe formule werd afgeleid, werd de GFR gemeten door middel van iothalamaat klaring (gemiddeld 68ml/min/1,72m2, SD = 40ml/min/1,73m2), en serum creatinine waarden (gemiddeld 145μmol/l) werden opnieuw gekalibreerd volgens de enzymatische methode van Roche die herleidbaar is naar de IDMS referentiemethode. De gemiddelde leeftijd van de populatie was 47 jaar, met een lage vertegenwoordiging van oudere patiënten; 9% van de proefpersonen was tussen 66 en 70 jaar oud, en slechts 3% was ouder dan 71 jaar. De formule werd verkregen uit een lineair regressiemodel voor de schatting van de logaritme van de GFR op basis van de verkregen creatininespiegels en met inbegrip van de variabelen leeftijd, geslacht en etnische groep. Er bestaan verschillende versies van de formule voor verschillende etnische groepen, en binnen die groepen bestaan verschillende formules afhankelijk van geslacht en creatininespiegel (tabel 1). De CKD-EPI-formule werd vervolgens gevalideerd in een onafhankelijke bevolkingsgroep met 3.896 personen uit 16 studies. Vergelijking van de nieuwe formule met MDRD-IDMS maakt duidelijk dat CKD-EPI betere resultaten oplevert, vooral voor hoge GFR-waarden. Tegelijkertijd is zij even nauwkeurig als MDRD-IDMS voor GFR-waarden onder 60ml/min/1,73m2 met een kleinere afwijking (mediaan verschil tussen gemeten en geschatte GFR van 2,5ml/min/1,73m2 vs 5,5ml/min/1,73m2), verbeterde precisie (intermediair verschil tussen gemeten en geschatte GFR van 2,5ml/min/1,73m2 vs 5,5ml/min/1,73m2) en een grotere nauwkeurigheid (intermediair verschil tussen gemeten en geschatte GFR van 2,5ml/min/1,73m2).73m2), verbeterde precisie (interkwartielafstand tussen verschillen = 16,6ml/min/1,73m2 vs 18,3ml/min/1,73m2) en grotere nauwkeurigheid (percentage geschatte GFR’s binnen 30% of minder van gemeten GFR = 84,1% vs 80,6%). Het gebruik van CKD-EPI in de NHANES (1999-2006) liet zien dat de mediane geschatte GFR 94,5 ml/min/1,73m2 was vergeleken met 85,0 geschat met MDRD-IDMS, waardoor de CKD-prevalentie 11,5% was in plaats van 13,1%; deze daling van de prevalentie werd hoofdzakelijk veroorzaakt door een daling van het aantal gevallen dat door MDRD-IDMS als stadium 3 CKD was geclassificeerd. Anderzijds is door de herindeling van patiënten volgens de CKD-EPI de prevalentie van CKD in stadium 1 gestegen, terwijl de prevalentie van CKD in stadium 2 en 3 is gedaald. De verspreiding van nieuwe formules voor de evaluatie van de GFR betekent dat deze formules moeten worden gevalideerd in populaties met verschillende klinische kenmerken. Het doel van onze studie was een aanzienlijk aantal patiënten met een breed scala aan GFR-waarden te verzamelen om de GFR-resultaten verkregen met behulp van de MDRD-IDMS en de nieuwe CKD-EPI-formule te vergelijken en te analyseren hoe dit de indeling in CKD-stadia beïnvloedde. Uit onze resultaten blijkt dat de nieuwe formule hogere waarden oplevert dan MDRD-IDMS. Deze verhoging van de GFR houdt in dat patiënten in mildere CKD-stadia worden heringedeeld; daartoe werd 9,8% van de gevallen die als 3B CKD waren ingedeeld, 3A, 17% van de 3A CKD-gevallen werd stadium 2 CKD, en 15,7% ging van stadium 2 naar stadium 1 CKD. Bovendien bleek uit analyse per leeftijdsgroep dat deze tendens naar mildere CKD-stadia groter was in de groep jonger dan 70; 18,9% van de proefpersonen ging van stadium 3B CKD naar stadium 3A, 34,1% van stadium 3A naar 2, en 24,0% van stadium 2 naar 1 CKD. Ondanks het feit dat slechts 3,7% van de proefpersonen die in de ontwikkeling van de CKD-EPI formule werden opgenomen ouder waren dan 70 jaar, is het percentage van overeenstemming dat voor deze groep in onze studie werd waargenomen groter dan 90% voor CKD stadia 2 tot 5; echter, onder degenen die door MDRDIDMS in CKD stadium 1 werden geplaatst, werd een groot aantal gevallen door de CKD-EPI formule ingedeeld als stadium 2 CKD. Wij denken dat een dergelijke herindeling in een stadium met een lagere GFR te wijten is aan het feit dat de MDRD-IDMS-formule voor sommige personen in deze populatie buitensporig hoge GFR-waarden oplevert. Deze waarden zijn moeilijk te geloven gezien de leeftijdsgebonden fysiologische afname van de GFR, en zijn het gevolg van de lage concentraties serumcreatinine die veel van deze patiënten hebben. De CKD-EPI-formule is beschikbaar in verschillende versies, afhankelijk van de creatininespiegel, zoals we in tabel 1 zien. Dit is om de resultaten beter te kunnen afstemmen op de werkelijke GFR-waarde die wordt verkregen door de iothalamaatklaring te meten. Het belangrijkste aspect van deze studie is dat het de eerste publicatie is waarin getracht wordt de nieuwe CKD-EPI formule in onze gemeenschap te valideren, en dat het gedaan werd in een groot patiënten cohort. We moeten echter in gedachten houden dat we de werkelijke GFR-waarde niet kennen, aangezien we niet over de middelen beschikken om deze rechtstreeks met een referentiemethode te meten. Deze voorafgaande taak werd echter reeds uitgevoerd in de oorspronkelijke publicatie, en daarom menen wij dat de resultaten grotendeels vergelijkbaar zijn. Onze resultaten komen overeen met die van Levey in die zin dat de patiënten in mildere stadia van CKD werden ingedeeld, wat vooral geldt voor de groep die door MDRD-IDMS als stadium 3 CKD werd ingedeeld. Deze resultaten zijn toe te schrijven aan kenmerken van de populatie die voor de CKD-EPI-formule werd gebruikt (personen met gemiddelde GFR-niveaus van 68 ml/min/1,73m2, vergeleken met 40 ml/min/1,73m2 in de groep die werd gebruikt voor de ontwikkeling van de MDRD-formule) en ook aan het gebruik van gestandaardiseerde methoden in vergelijking met de referentiemethode voor het meten van serumcreatinine. In de handleidingen voor de klinische praktijk die onlangs door de SEN in samenwerking met de Spaanse vereniging voor gezins- en gemeenschapsgeneeskunde (semFYC)42 zijn opgesteld, staat dat verwijzing naar een nefroloog wordt geadviseerd voor patiënten jonger dan 70 jaar met een GFR lager dan 45ml/min/1,73m2. Onze resultaten wijzen erop dat een groot aantal patiënten die momenteel worden beschouwd als kandidaten voor verwijzing, niet langer kandidaten zouden zijn. Dit zou belangrijke gevolgen hebben voor de sociale gezondheidszorg, aangezien het de congestie in de nefrologie-eenheden zou helpen verminderen. Ondertussen kunnen wij blijven werken aan de verbetering van de nauwkeurigheid en precisie van de GFR-meet- en -schattingsmethoden. Verder zijn wij van mening dat een andere belangrijke factor die in overweging moet worden genomen bij de evaluatie van nieuwe geschatte GFR-formules de beoordeling is van hun potentieel als prognostische factoren voor hart- en vaatziekten en/of overleving.
Acknowledgements
Deze studie werd uitgevoerd met steun van het Spaanse Netwerk voor Nefrologisch Onderzoek (REDinREN) 16/06. RETICS. Carlos III Instituut voor Gezondheidsonderzoek. Madrid, Spanje.

Tabel 1. Geschatte glomerulaire filtratiesnelheid formule CKD-EPI
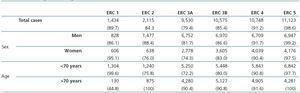
Tabel 2. Demografische kenmerken van de populatie uitgesplitst naar geslacht en leeftijd, met verdeling naar leeftijdsgroep
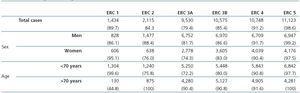
Tabel 3. Overeenstemming in de CKD-stadiumclassificaties voor geschatte glomerulaire filtratiesnelheden (GFR) met behulp van de MDRDIDMS- en CKD-EPI-formules

Tabel 4. Overeenstemmingen (vetgedrukt in zwart) bij de indeling van stadia van chronische nierziekte (CKD) voor glomerulaire filtratiesnelheid (GFR) geschat met behulp van de MDRD-IDMS- en CKD-EPI-formules, met de GFR volgens MDRD-IDMS als referentie en rekening houdend met geslacht en

Tabel 5. Waarden voor serumcreatinine en glomerulaire filtratiesnelheid geschat met de MDRD-IDMS- (GFRMDRD-IDMS) en CKDEPI- (GFRCKD-EPI)-formules voor verschillende stadia van chronische nierziekte (CKD) en concordantieanalyse van GFRCKD-EPI en GFRMDRD-IDMS met behulp van de
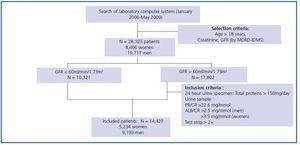
Figuur 1.